L'ONCOTEST
Nous sommes parvenus en 1979. I1 y a un an, Beljanski et ses collaborateurs ont dû
quitter
l'Institut Pasteur; la rupture a été violente. Ils sont maintenant à la Faculté de
Pharmacie de
Châtenay -Malabry.
Des idées entièrement nouvelles au sujet du cancer et de ses mécanismes ont germé
dans l' esprit
de Mirko Beljanski et se font de plus en plus précises. I1 ne les publiera cependant que
plus tard.
En attendant, après avoir constaté que certaines molécules agissent uniquement sur
la
réplication de 1'ADN provenant de tissus sains, tandis que d'autres substances, et en
particulier
des cancérogènes bien connus, stimulent très spécifiquement la synthèse d'ADN
d'origine
cancéreuse, Beljanski met au point l'Oncotest. I1 est destiné en premier lieu à la
détection des
cancérogènes mais il sera, entre les mains de l'équipe, un outil d' application plus
générale et
de première importance.
Jusqu'au début des années 70, les potentialités cancérogènes d'un produit étaient
évaluées au
moyen d'essais sur l'animal. Ce procédé de contrôle est. du reste, toujours employé,
bien qu'au
fil des ans il soit apparu de plus en plus clairement que ces essais ne sont pas
facilement
extrapolables à l'homme.
Aussi le test dont Ames, aux Etats-Unis, annonça la mise au point en 1973 fut-il vite
adopté;
ce type de test est depuis lors systématiquement utilisé, en particulier pour les
nouvelles
molécules pharmaceutiques.
Le test d'Ames est le reflet de son temps. I1 est fondé sur la conviction,
contemporaine de sa
mise au point mais ébranlée de nos jours, que la cancérisation trouve son origine dans
une
mutation qui transforme un ADN normal en ADN tumoral. I1 fait appel à des bactéries,
microorganismes à partir desquels se bâtissaient les théories nouvelles de la biologie
moléculaire, et aux microsomes hépatiques, autre centre d'intérêt des biologistes, qui
en
attendaient beaucoup.
La substance à étudier est d' abord activée au moyen des nombreuses enzymes
contenues dans la
fraction microsomale extraite de foie de rat. Puis elle est mise en présence d'un mutant
de
Salmonella typhimurEum qui, contrairement à la souche sauvage, ne peut pas se développer
sur
un milieu de culture dépourvu d'histidine, car il ne synthétise pas cet acide aminé
(souche his-).
En présence d'un cancérogène, cette bactérie subit une mutation, toujours la même,
qui la
ramène au type sauvage d'origine (his+), qui synthétise l'histidine. Les résultats
s'obtiennent
en quelques jours. Cependant, Ames lui-même s'était rendu compte, dès le début, que 20
% des
cancérogènes connus ne sont pas mutagènes.
L'Oncotest, inventé par Beljanski vers 1976 et décrit pour la première fois dans un
article
datant de 1979, est radicalement différent du test d'Ames.
I1 est fondé sur la comparaison de la réplication in vitro d'ADN de tissus sains et
de tissus
cancéreux d'un organe de même type en présence du composé à tester. I1 s'appuie sur
une
observation maintes fois répétée au cours des expériences de l'équipe et jamais prise
en défaut:
les substances bien connues pour leurs propriétés cancérogènes stimulent fortement et
spécifiquement la réplication de 1'ADN cancéreux. Durant les mois où il met au point
ce test,
le mécanisme et les causes de cette action se feront de plus en plus clairs aux yeux de
Beljanski.
Deux ans après, il sera prêt à publier son interprétation totalement nouvelle de la
nature du
processus cancereux.
Dans l'Oncotest, des ADN purifiés d'origine humaine (biopsies et prélèvements per-
opératoires), les uns provenant d'organes sains: poumon, sein, ovaire, cerveau, les
autres isolés
à partir d'organes cancéreux correspondants, sont incubés dans des conditions
strictement
identiques"'. Parmi les constituants habituels du milieu d'incubation se trouvent,
d'une part, un
désoxyribonucléoside-S'-triphosphate marqué à la thymidine tritiée, qui, une fois
incorporé à
1'ADN nouvellement formé, va permettre d'en mesurer la quantité, et, d'autre part, une
ADN
polymérase ADN dépendante extraite d'E. coli, qui va présider à la synthèse de cet
ADN
nouveau à partir de 1'ADN fourni comme matrice.
L'ADN synthétisé est précipité par l'acide trichloracétique et sa radioactivité
est mesurée avec
un compteur. Pour juger de l' action d' une substance, la quantité d'ADN synthétisé, d'
une part,
à partir d'ADN normal, d'autre part à partir d'ADN cancéreux, est d'abord évaluée
avant
addition du produit à tester, puis lorsqu'il est présent.
Une forte stimulation de la synthèse des ADN cancéreux, accompagnée d'une très
faible action
sur les ADN normaux, indique que le produit essayé est cancérogène.
La différence observée dans ce cas est sans équivoque: la synthèse d'ADN cancéreux
est de
cinq à dix fois supérieure à celle d'ADN sain.
La technique est classique, relativement peu onéreuse. Les quantités de produits
nécessaires
pour un essai sont minimes: de 0,5 à 1 microgramme d'ADN; de 40 à 80 microgrammes
d'enzyme; de 0,5 à 60 microgrammes de substance à tester. La sensibilité de l'Oncotest
est
même telle qu'il détecte un centième de microgramme d'aflatoxine B1, dangereux
cancérogène
capable de provoquer des cancers du foie.
La réponse s'obtient en deux à quatre heures, alors que les délais, dans le test
d'Ames, sont de
l'ordre d'une semaine.
La fiabilité de l'Oncotest a été confirmée par des épreuves répétées
effectuées au moyen de
plus de vingt cancérogènes connus pour donner des réponses positives dans le test d'
Ames et
employés à des concentrations variées.
(1) Le principe de l'Oncotest est d'une application très générale; selon les
besoins, des ADN de provenance très
diverses peuvent être choisis. Il est même utilisable avec les ADN des souches
bactériennes his- et his+ du test
d'Ames: dans tous les cas, tous les cancérogènes donnent une réponse positive; nous
verrons plus loin pourquoi.
< IMG_P38.JPG >

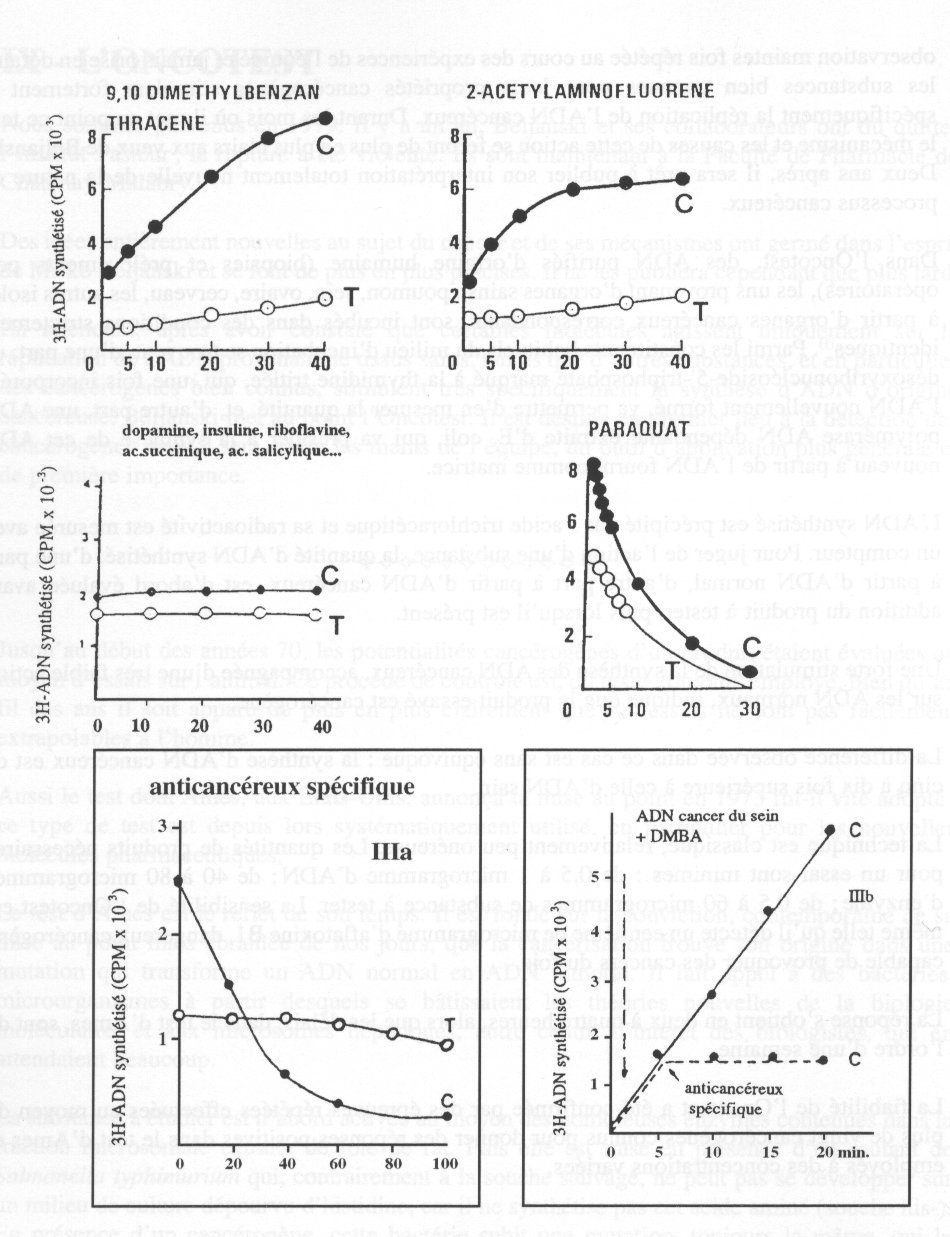
ONCOTEST:
: stimulation préférentielle de la synthèse in vitro d'ADN des tissus cancéreux par
les cancérogènes.
: effet des substances neutres.
: effet des substances toxiques.
: inhibition préférentielle de la synthèse in vitro D'ADN des tissus cancéreux par un
anticancéreux
spécifique.
: anticancéreux spécifique déplaçant le cancérogène et inhibant son effet stimulant
(réf.95).
= ADN cancéreux.
= ADN normal témoin.
L'Oncotest, plus rapide et plus sensible que les autres tests habituellement utilisés,
présente
encore d'autres avantages. En effet, il permet de mettre en évidence les potentialités
cancérogènes des composés qui échappent à la détection par le test d' Ames et
doivent alors
subir des mois de coûteux essais sur l' animal de laboratoire. Des cancérogènes comme
l'éthionine, l'actinomycine D, la bléomycine, détectés par leurs effets chez l'
animal, mais non
par le test d'Ames, donnent des réponses positives avec l'Oncotest.
D'autre part, l'Oncotest confirme clairement que les hormones stéroïdes, qui ne
donnent pas
non plus de réponse positive dans le test d'Ames, peuvent, quand elles sont présentes en
quantités supérieures aux taux physiologiques, se comporter comme des cancérogènes,
mais
uniquement vis-à-vis de leurs organes-cibles: elles stimulent fortement la réplication
d'ADN
cancéreux de sein ou d'ovaire. C'est bien ce que la médecine constate.
Mais l'Oncotest offre encore d'autres possibilités. I1 indique si une molécule, qui
n'est pas
cancérogène, a néanmoins des effets toxiques: dans ce cas, elle inhibe l'action de
1'ADN
polymérase et la réplication est stoppée. C' est ce que font des désherbants comme le
diquat ou
le paraquat. L'Oncotest donne aussi la garantie qu'un produit est "neutre", s'il
n'exerce pas
d'action au niveau de la réplication de 1'ADN. Le cholestérol, la saccharine pure sont
des
substances neutres.
Enfin, l'Oncotest a servi à Beljanski d'épreuve pour découvrir des anticancéreux spécifiques.
Sur 200 molécules soumises au nouveau test, plus de 35 % se sont révélées
cancérogènes. I1
faut savoir qu'à faibles doses, presque toutes les molécules utilisées en
chimiothérapie
anticancéreuse se comportent comme de véritables cancérogènes, ce que le test d' Ames
indiquait déjà pour nombre de ces produits. Or, quand une période de chimiothérapie
est
achevée, l'organisme élimine peu à peu l'antimitotique; il sera de ce fait, à un
moment donné,
présent dans le corps en doses faibles et aura des effets exactement contraires à ceux
qui étaient
recherchés au départ.
Beljanski a maintes fois tenté d'intéresser à l'Oncotest des organismes
scientifiques et des
industriels: en pharmacie, en agro-alimentaire, il rendrait d'immenses services et serait
la
source d'économies considérables de temps et d'argent. En vain.
I1 a même été reproché à l'Oncotest d'être trop sensible... Dans bien des cas, en
effet, des
substances considérées comme dépourvues de potentialités cancérogènes ont donné des
réponses positives: l'équipe a prouvé qu'elles étaient dues à la présence
d'impuretés, en
quantités certes infimes, mais dangereuses. L'Oncotest donne donc la possibilité de
vérifier la
pureté des produits employés.
RÉSUMÉ
Peu après son arrivée à la Faculté de Pharmacie de Châtenay-Malabry, Beljanski
annonce la mise au point de l'Oncotest, destiné à la détection des substances
cancérogènes.
Pendant longtemps, celles-ci n'avaient pu être décelées qu'au moyen d'une
expérimentation animale longue et coûteuse, diffficile à extrapoler à l'homme. A
partir
des années 70 fut adopté le test d'Ames, dans lequel, cependant, 20 % des
cancérogènes connus ne donnent pas de réponse positive.
Radicalement différent, I' Oncotest se fonde sur un phénomène régulièrement
observé
par l'équipe Beljanski: les substances bien connues pour leurs propriétés
cancérogènes stimulent fortement et spécifiquement la réplication de 1'ADN des
tissus cancéreux, mais pratiquement pas celle de 1'ADN des tissus sains
correspondants .
Ce test biochimique est simple de principe et d'emploi. Dans un milieu d'incubation
approprié, le produit à tester est mis successivement en présence d'ADN humains
cancéreux et normaux d'organes différents: poumon, sein, ovaire, cerveau (provenant
de biopsies ou de prélèvements per-opératoires). Si le produit est cancérogène, la
synthèse d'ADN cancéreux sera de cinq à dix fois supérieure à celle d'ADN normal.
La fiabilité de l'Oncotest est démontrée par une longue expérimentation.
Les quantités nécessaires de réactifs et de substance à tester sont minimes, de
l'ordre
du microgramme, et le test peut détecter jusqu'à un centième de microgramme
d'aflatoxine B1, hautement cancérogène pour le foie. La réponse s'obtient en deux à
quatre heures, au lieu d'une semaine pour le test d'Ames; elle est positive pour les
cancérogènes que ce dernier ne peut déceler. Les hormones stéroides, en particulier,
réagissent avec les ADN de leurs organes-cibles (sein et ovaire).
L'Oncotest peut également indiquer si une substance, sans être cancérogène, est
néanmoins toxique, ou si elle est "neutre", sans effet sur 1'ADN.
I1 confirme également que les antimitotiques, quand ils sont présents à faibles doses
- ce qui se produit, à la suite d'une chimiothérapie, au cours de leur élimination par
l'organisme - se comportent comme de véritables cancérogènes.
En outre, le test montre que, souvent, des substances non dangereuses par elles-
mêmes contiennent cependant des impuretés cancérogènes.
Enfin, l'Oncotest et ses variantes (utilisation d'ADN d'autres provenances) ont été
employés par Beljanski pour découvrir des anticancéreux spécifiques.
Ce test, qui rendrait d'immenses services dans des domaines comme la
pharmacologie ou l'agro-alimentaire, n'a pourtant pas retenu l'attention des
organismes scientifiques ni des industriels, sans doute pour des raisons ayant peu de
rapport avec la science.